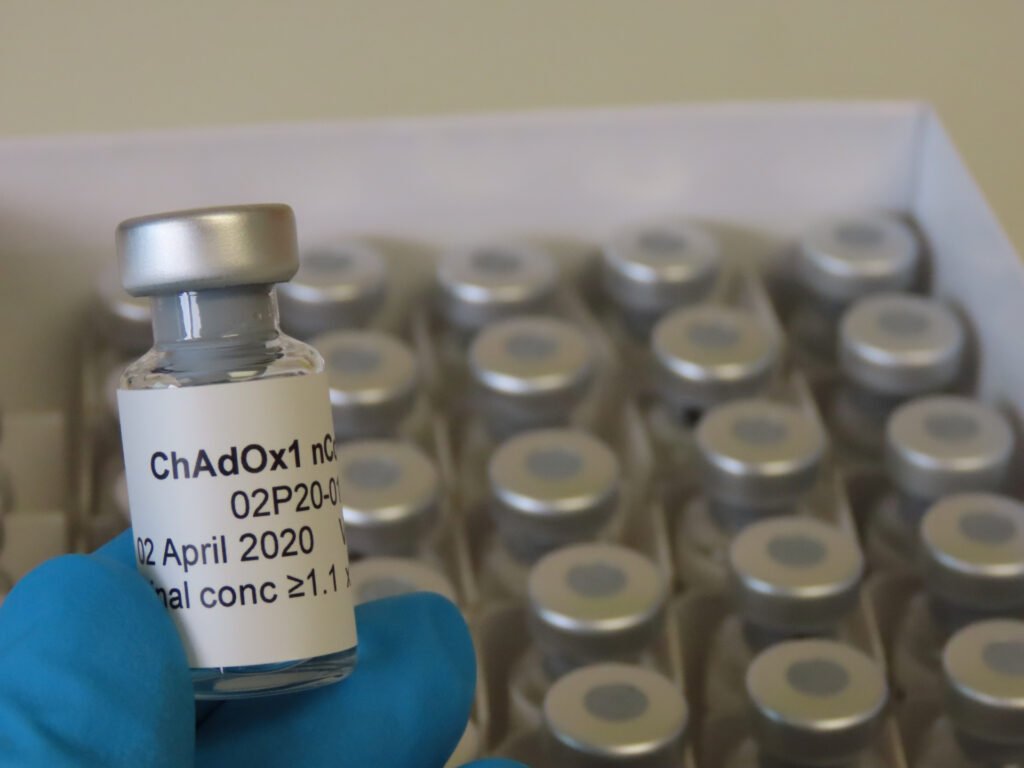
Nesta quinta-feira (01), a empresa farmacêutica AstraZeneca enviou à Agência Nacional de Vigilância Ambiental (Anvisa) os primeiros documentos para iniciar o registro no Brasil da vacina desenvolvida em parceria com a Universidade de Oxford contra Covid-19.
Agora, a agência reguladora tem um prazo de 20 dias para analisar a remessa inicial de dados, referentes aos estudos não clínicos. O procedimento foi possível depois que Anvisa protocolou uma nota técnica com orientações para submissão continuada de documentação técnica para análise com caráter de urgência, a fim de acelerar as etapas de aprovação de vacinas contra a Covid-19. A adaptação no envio das informações consiste em possibilitar que as empresas produtoras dos imunizastes possam registrar novos dados parceladamente, à medida em que novidades vão surgindo.

A nota técnica instrui: “O número de ciclos de aditamentos dependerá do número de pacotes a serem submetidos pela empresa interessada, não havendo limite imposto pela Anvisa. Recomendamos que a empresa não fique aguardando a juntada de determinada quantidade de documentos para então submetê-los à agência, uma vez que isso desvirtua o propósito do procedimento, que é o de dar maior celeridade à análise”.
Normalmente, todos os dados sobre a eficácia, segurança, qualidade de um medicamento e os demais documentos necessários são apresentados no início da avaliação de registro, quando já há todos os procedimentos concluídos. No caso da “submissão contínua”, a Anvisa irá analisar os dados de acordo com a disponibilidade dos mesmos.
“Isso não significa que já se possa chegar a uma conclusão sobre a qualidade, segurança e eficácia da vacina, pois muitos dados ainda precisam ser submetidos à análise”, alerta a agência.
Ainda segundo a Anvisa, a “submissão contínua” continuará até que evidências suficientes estejam disponíveis para suportar um pedido formal de registro. Via Diário de Pernambuco